2.1.1.4 Prędkość cząsteczek
Ponieważ ruch cząsteczek pomiędzy zderzeniami jest zupełnie chaotyczny i przypadkowy operuje się wartościami średnimi drogi swobodnej i szybkości.
Średnia
droga swobodna jest to przeciętna odległość jaką cząsteczka przebywa
pomiędzy dwoma kolejnymi zderzeniami.
Zgodnie z teorią Maxwella-Boltzmanna statystyczny rozkład szybkości cząsteczek gazu w danej temperaturze T dany jest równaniem:
gdzie
energia kinetyczna cząsteczki wynosi:
![]() , a k jest
wielkością stałą zwaną stałą
Boltzmanna (II.2.1.1.3). Rys. 2.03
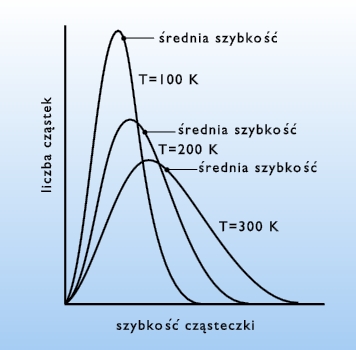
przedstawia graficzny obraz tego rozkładu. Położenie maksimum na
krzywej rozkładu zależy od temperatury (rys. 2.04). Wraz z jej wzrostem rośnie
ilość cząsteczek o większej
szybkości.
, a k jest
wielkością stałą zwaną stałą
Boltzmanna (II.2.1.1.3). Rys. 2.03
przedstawia graficzny obraz tego rozkładu. Położenie maksimum na
krzywej rozkładu zależy od temperatury (rys. 2.04). Wraz z jej wzrostem rośnie
ilość cząsteczek o większej
szybkości.
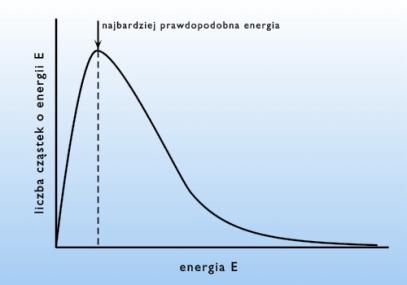
Rys.2.03 Rozkład energii cząsteczek gazu w danej temperaturze (rozkład Maxwella-Boltzmanna).