Co po co Geologowi wiedza o strukturze elektronowej atomu?
1. Elektronowa struktura atomu
1.3. Powłoki elektronowe i konfiguracja powłokowa
Elektrony o zbliżonych wartościach energii tworzą powłokę elektronową. Elektrony należące
do danej powłoki znajdują się w przestrzeni (warstwie) zawartej między dwiema
sferami o wspólnym środku, w obrębie której najczęściej się poruszają. Granice
pomiędzy poszczególnym powłokami nie są ostre, a zatem wzajemnie się one przenikają.
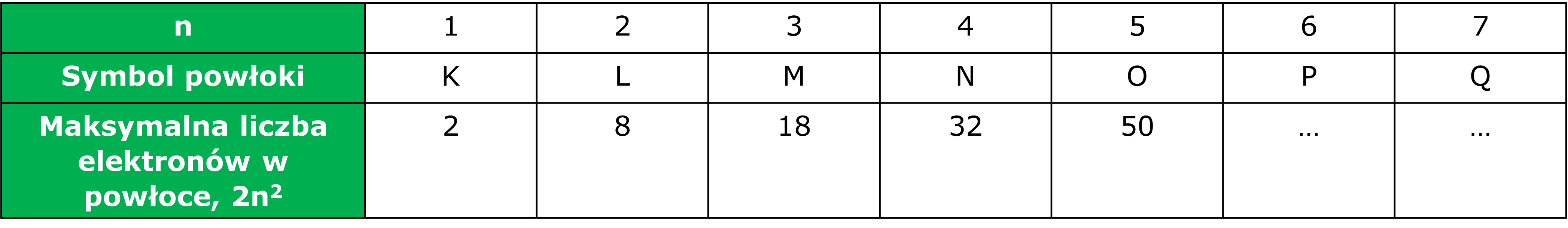
Liczba powłok elektronowych poznanych dotychczas pierwiastków nie przekracza siedmiu (siedem okresów w układzie okresowym). Numerację powłok elektronowych rozpoczyna się od powłoki najbliższej jadra, nadając im równocześnie odpowiednie symbole literowe.
Im więcej elektronów posiada dany atom tym więcej zapełniają one powłok. Przy czym powłoka elektronowa może być zajęta przez elektrony całkowicie, częściowo lub niezajęta. Im wyższy numer powłoki tym dalej od jądra znajduje się odpowiadająca mu warstwa i tym słabsze są siły wiążące elektrony z jądrem.
Maksymalna liczba elektronów w powłoce jest określana iloczynem 2n2, w którym n oznacza numer powłoki (równy głównej liczbie kwantowej), zatem powłoka pierwsza może zawierać 2 elektrony, powłoka druga – 8, itd.
Konfiguracja powłokowa to rozmieszczenie elektronów w powłokach. Zapisywana z wykorzystaniem literowych symboli powłok zajętych przez elektrony i liczby elektronów w poszczególnych powłokach podawanej z prawej strony danego symbolu powłoki w indeksie górnym.
Przykład:
20Ca: K2L8M8N2
Konfiguracja powłokowa jest łatwa do ustalenia tylko w przypadku pierwiastków grup głównych. W przypadku pierwiastków grup poboczny oraz lantanowców i aktynowców algorytm opisany poniżej nie może być stosowany.
Etapy ustalania konfiguracje powłokowej dla pierwiastków grup głównych:
- Ustalić liczbę obsadzanych powłok elektronowych (równa numerowi okresu, w którym leży dany pierwiastek),
- Wpisać liczbę elektronów dla ostatniej powłoki (równa liczbie jedności w numerze grupy, w której leży dany pierwiastek),
- Dla powłok, poza przedostatnią, wpisać maksymalne liczby elektronów, wynikające ze wzoru 2n2,
- Liczbę elektronów w przedostatniej powłoce obliczyć odejmując od liczby atomowej liczbę elektronów obsadzoną już na pozostałych powłokach.
Jeżeli obliczona w ten sposób liczba elektronów w przedostatniej powłoce wyjdzie ujemna, co ma miejsce w przypadku Cs, Ba, Fr, Ra, to należy przyjąć dla niej osiem elektronów, a liczbę elektronów na powłoce trzeciej od końca obliczyć, odejmując od liczby atomowej liczbę elektronów na pozostałych powłokach.
Przykład:

