Kształt cząsteczek
1. Teoria VSEPR
1.3. Wartość liczby przestrzennej a struktury przestrzenne drobin
Liczba przestrzenna 2, symetria kierunków orbitalnych liniowa (diagonalna), LwpE = 0
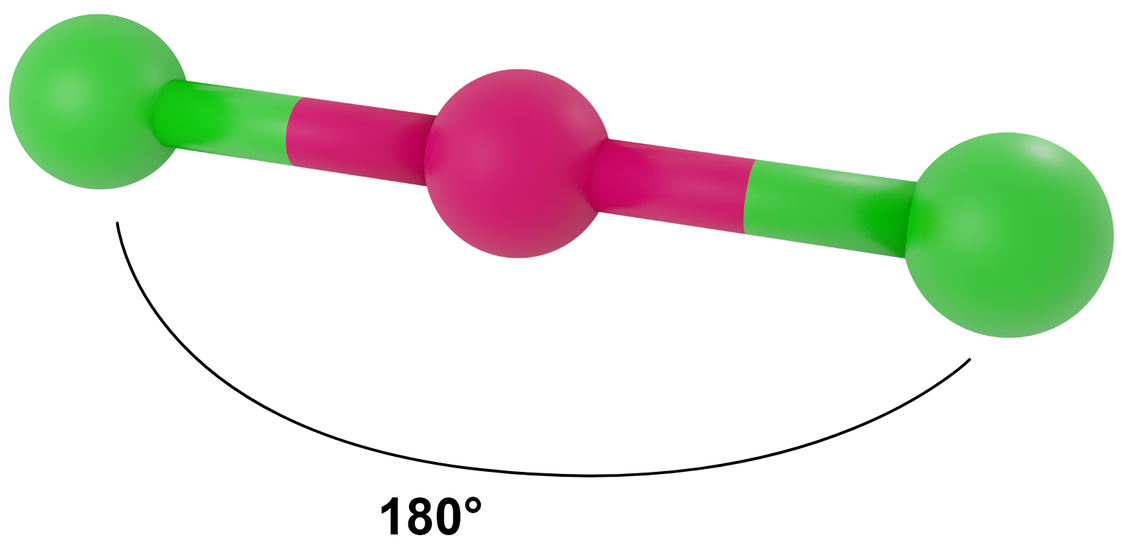
Przykłady: BeCl2, CO2
Liczba przestrzenna 3, symetria kierunków orbitalnych trygonalna
- dla LwpE = 0 - trójkąt równoboczny
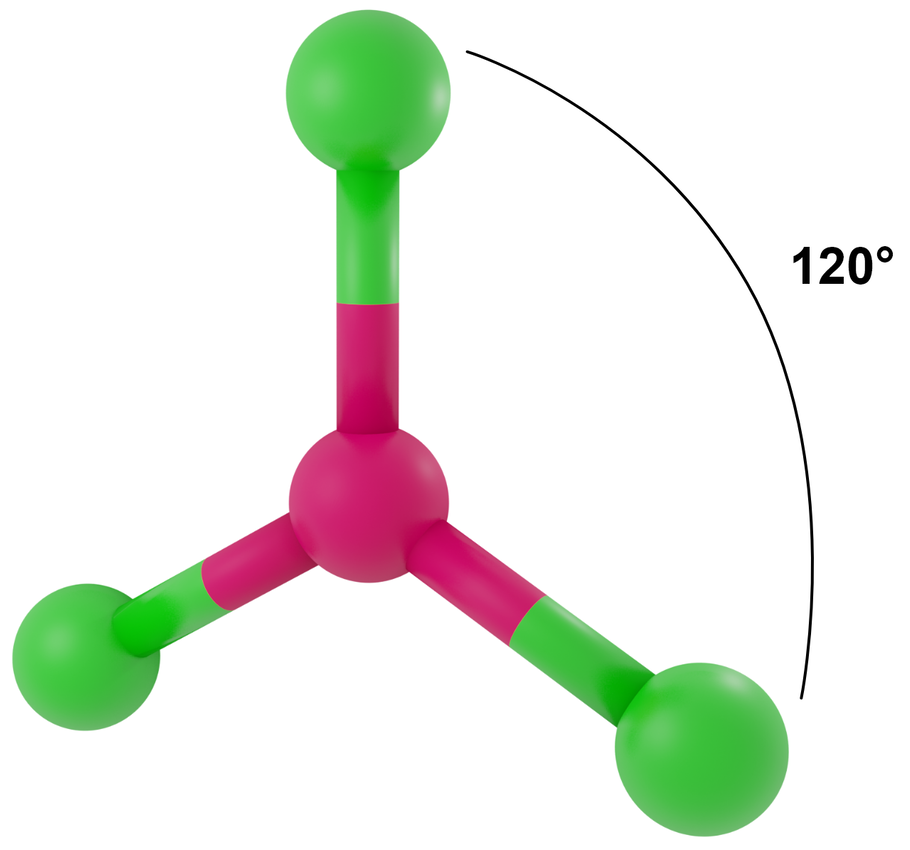
Przykłady: BF3, CO32-, NO3-, SO3
- dla LwpE = 1 - trójkąt równoramienny
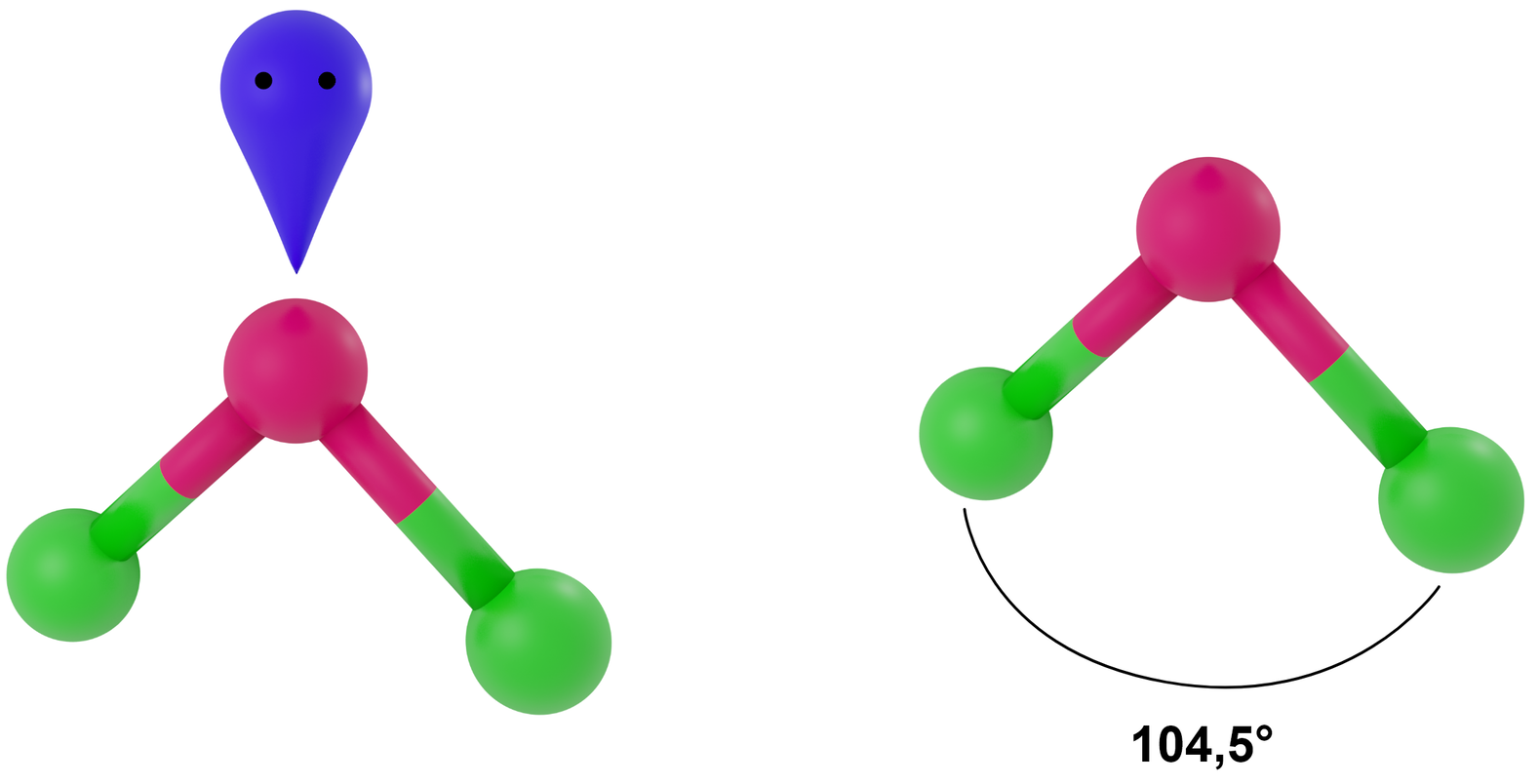
Przykłady: NO2-, SO2, O3
Liczba przestrzenna 4, symetria kierunków orbitalnych tetraedryczna
- dla LwpE = 0 - tetraedr
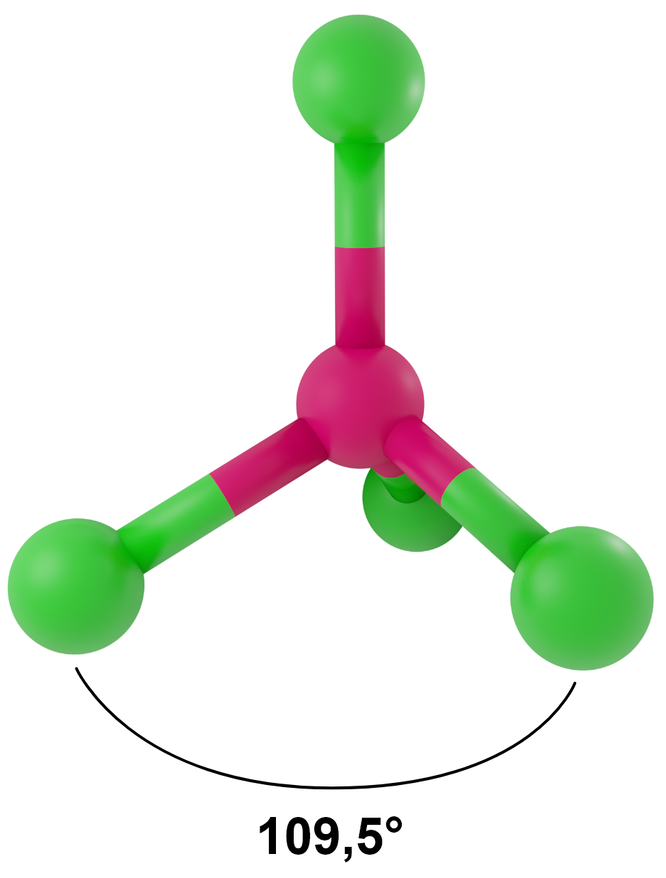
Przykłady: CH4, PO43-, SO42-, ClO4-
- dla LwpE = 1 - piramida trygonalna
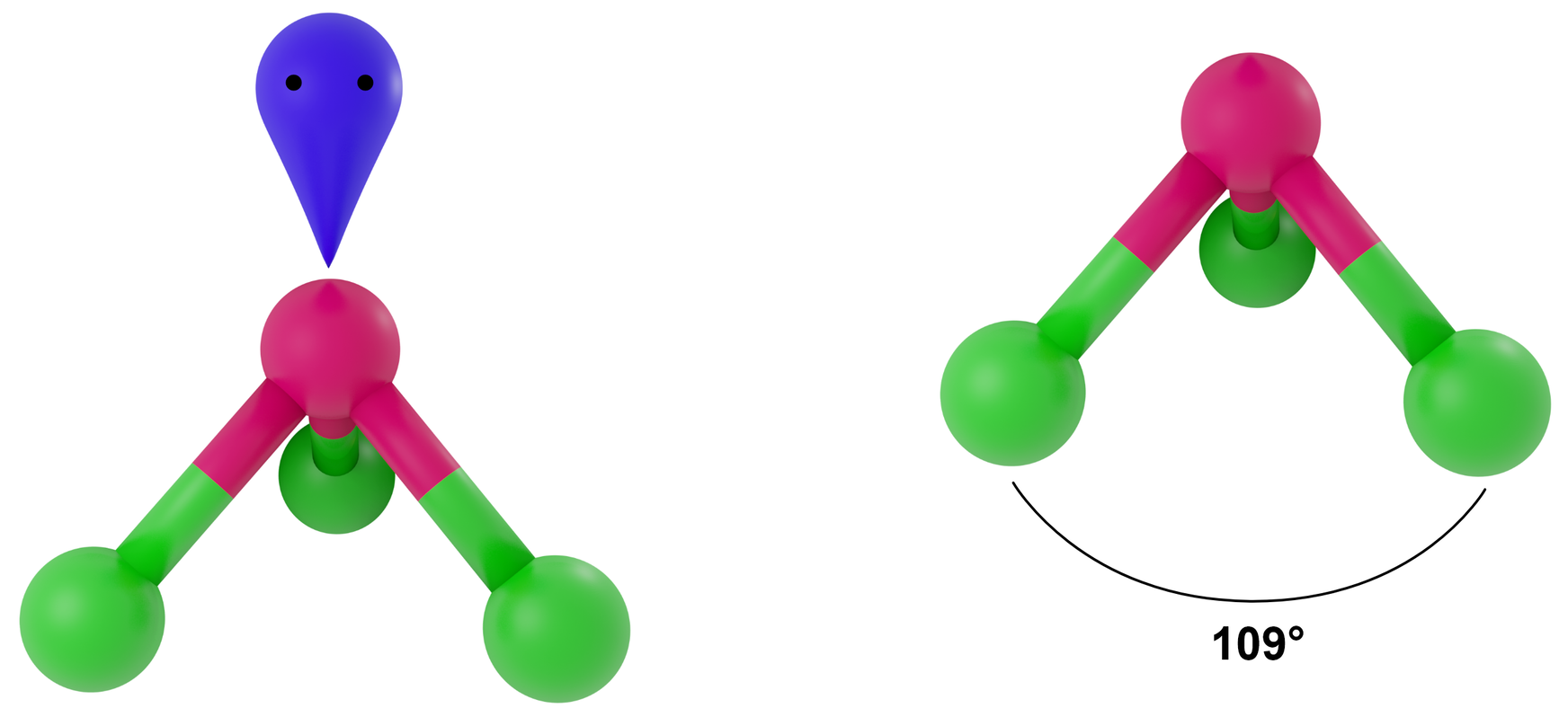
Przykłady: NH3, PCl3
- dla LwpE = 2 - trójkąt równoramienny
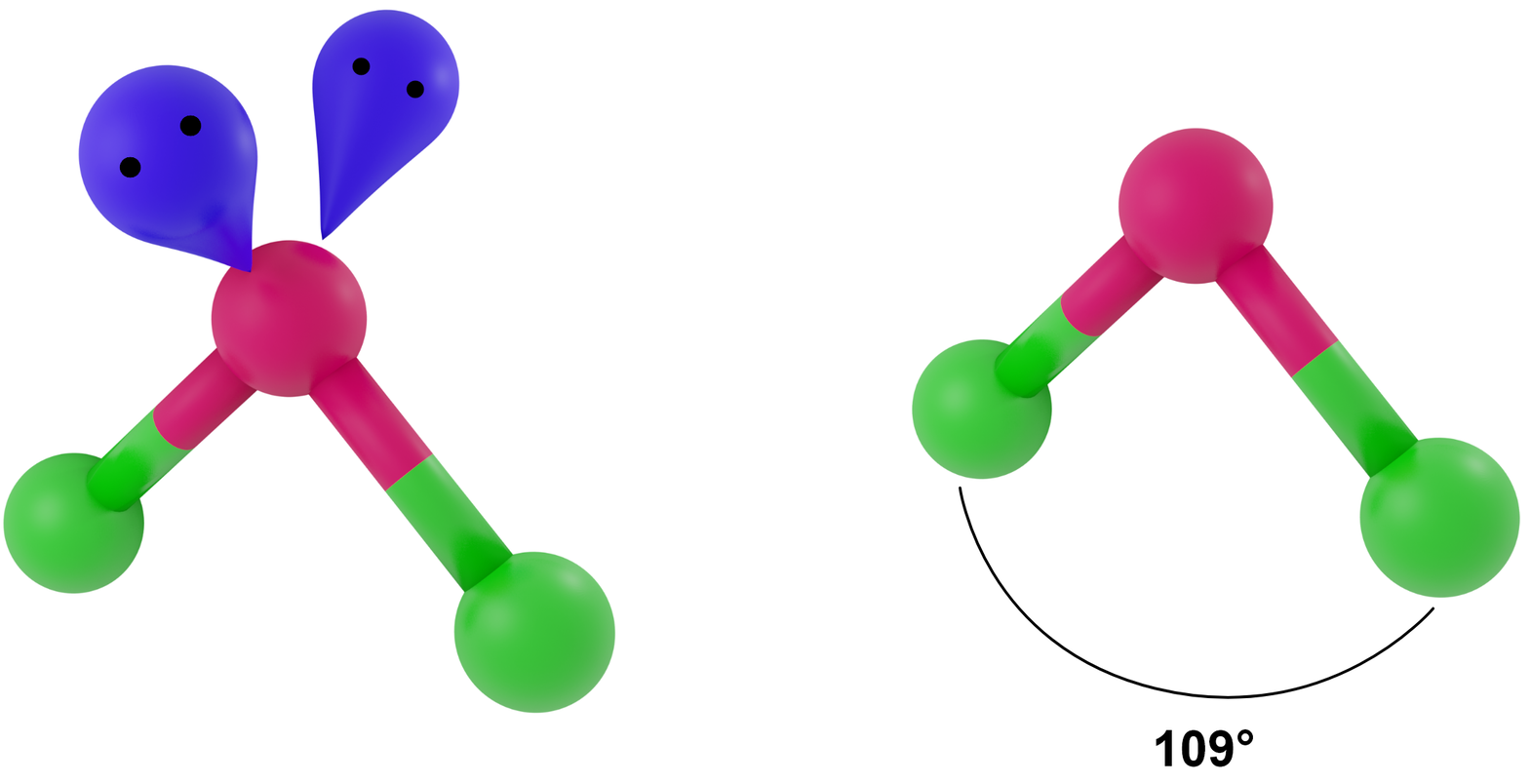
Przykłady: H2O, OF2
Liczba przestrzenna 5, symetria kierunków orbitalnych bipiramidy trygonalnej
- dla LwpE = 0 - bipiramida trygonalna
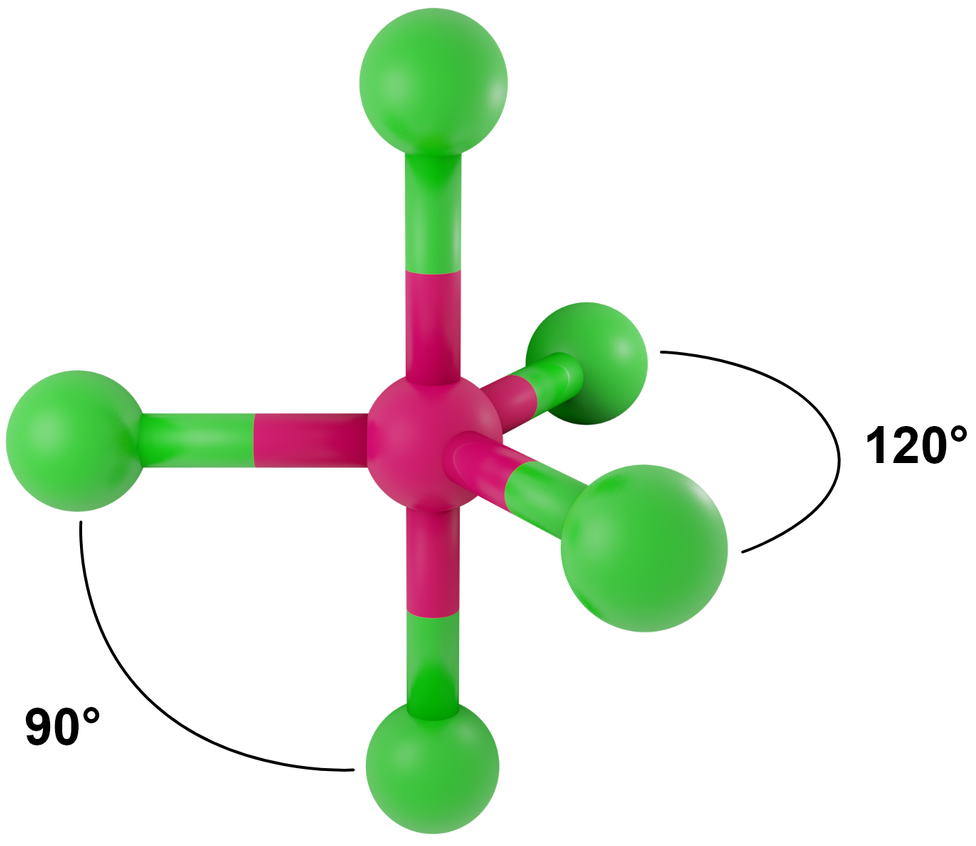
Przykłady: PCl5
- dla LwpE = 1 - zdeformowany tetraedr

Przykłady: SF4
- dla LwpE = 2 - deltoid wypukły
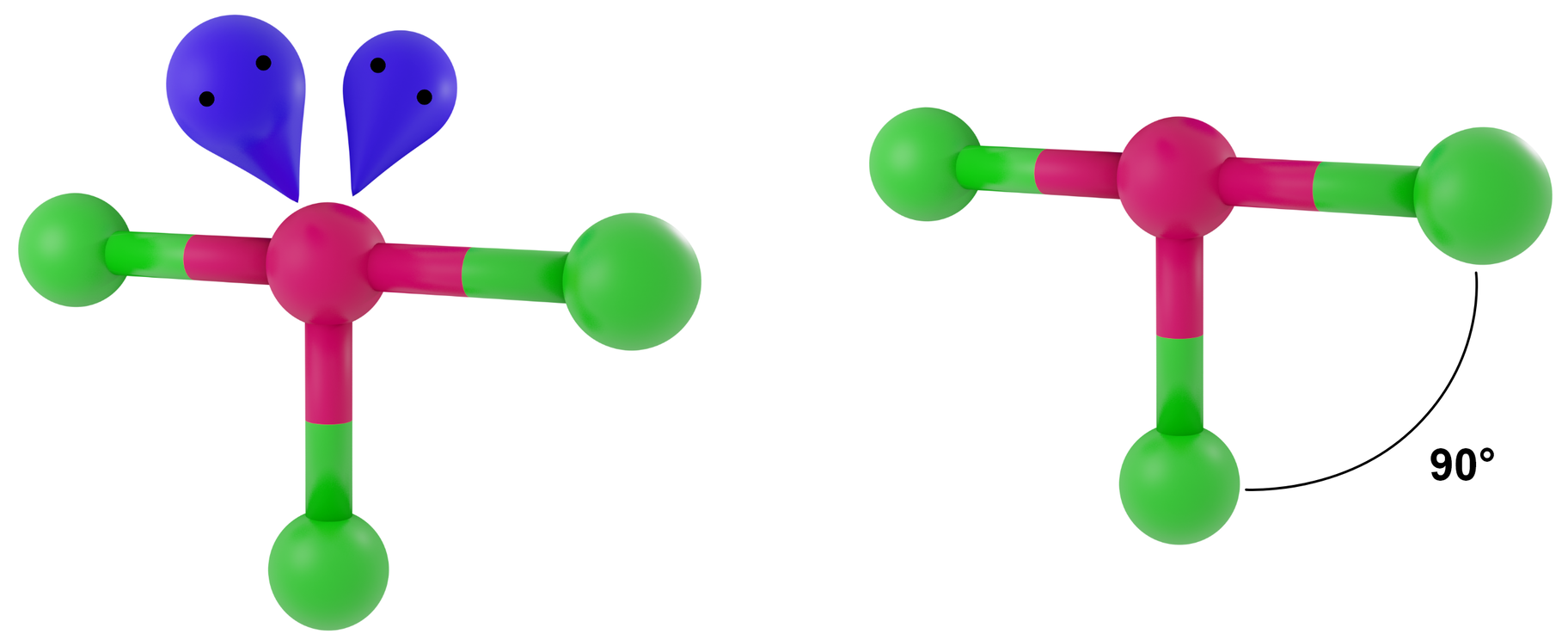
Przykłady: ClF3, BrF3
- dla LwpE = 3 - liniowa
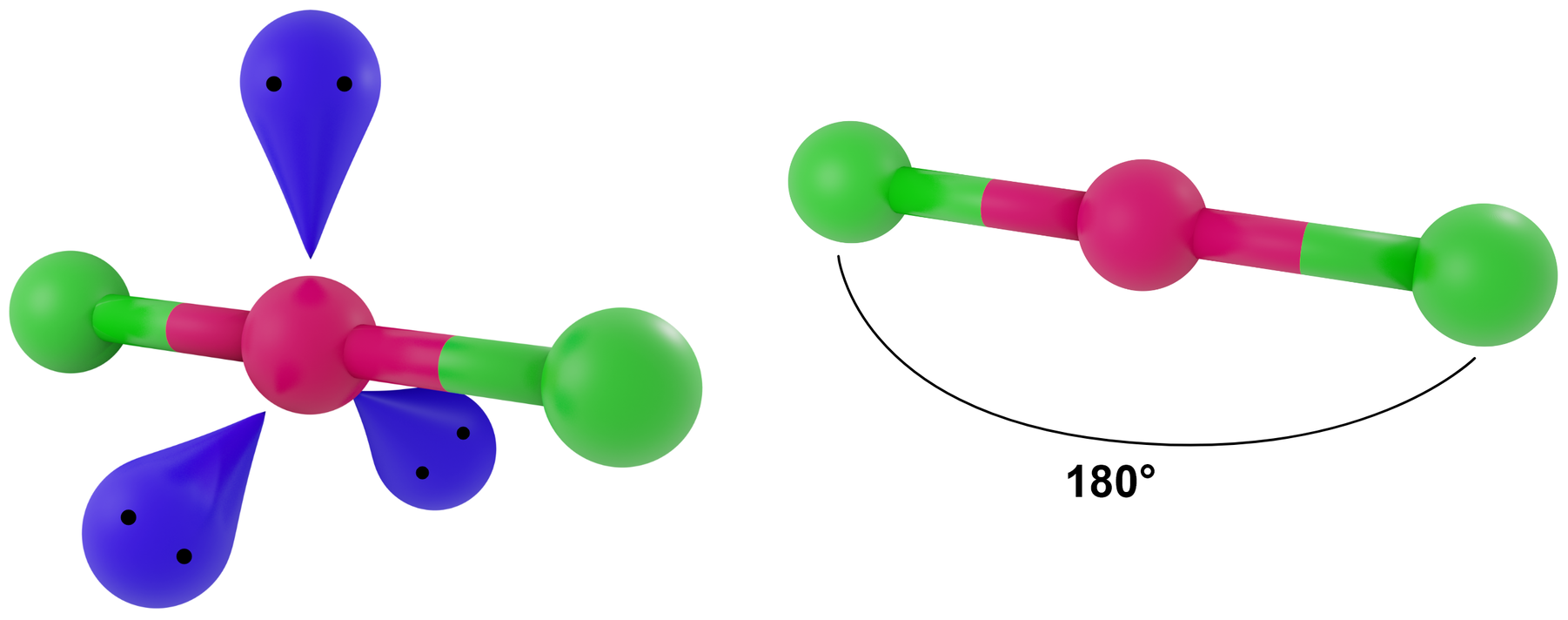
Przykłady: XeF2, ICl2-
Liczba przestrzenna 6, symetria kierunków orbitalnych bipiramidy tetragonalnej (oktaedru)
- dla LwpE = 0 - bipiramida tetragonalna (oktaedr)
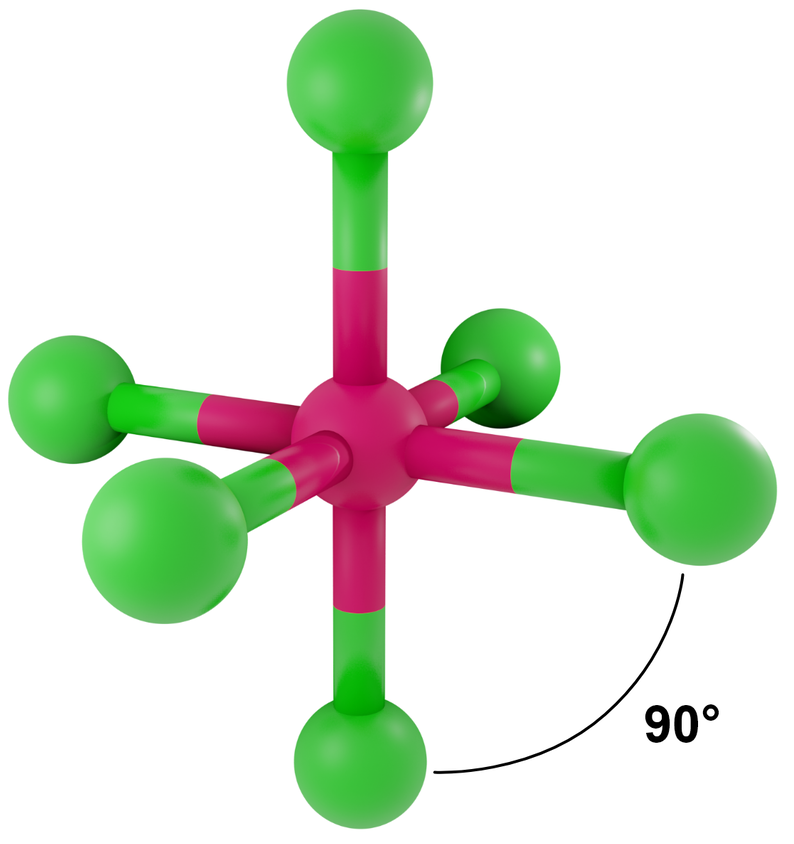
Przykłady: SF6
- dla LwpE = 1 - piramida tetragonalna
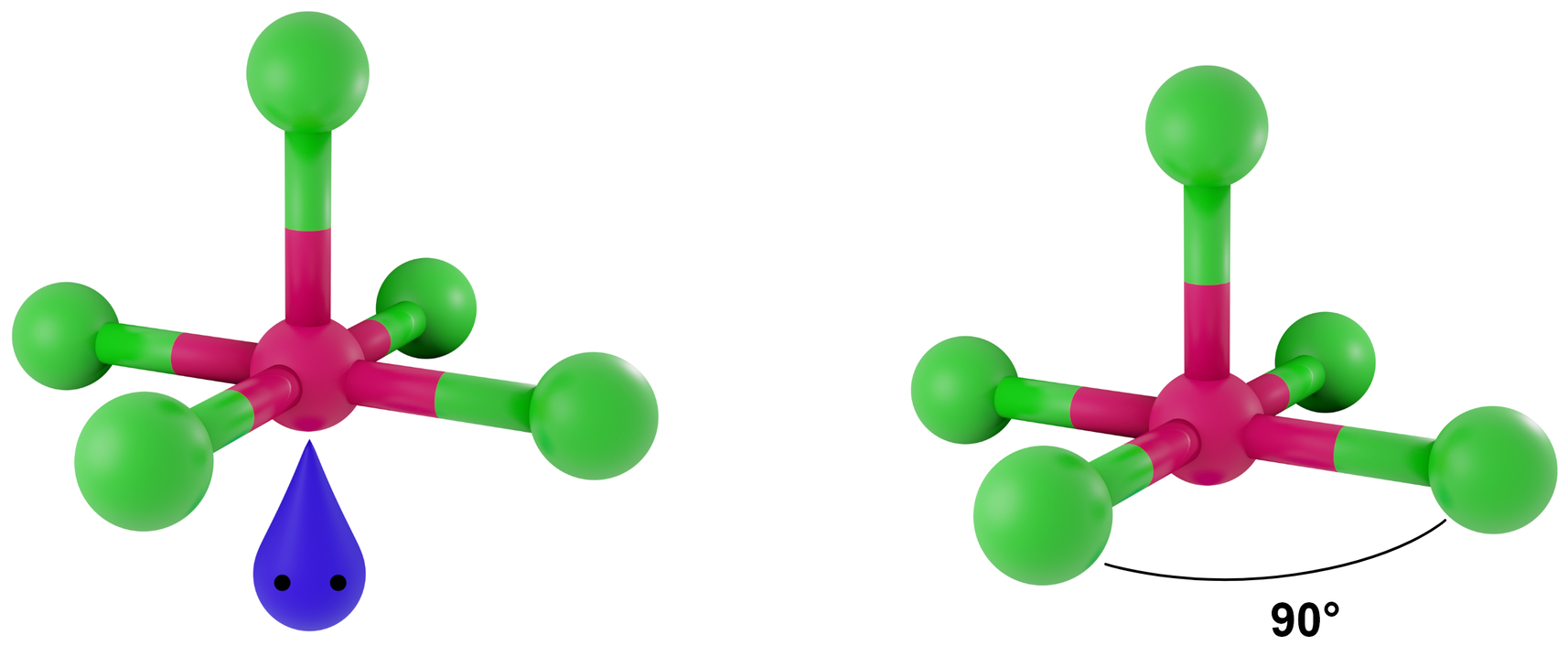
Przykłady: IF5
- dla LwpE = 2 - kwadrat
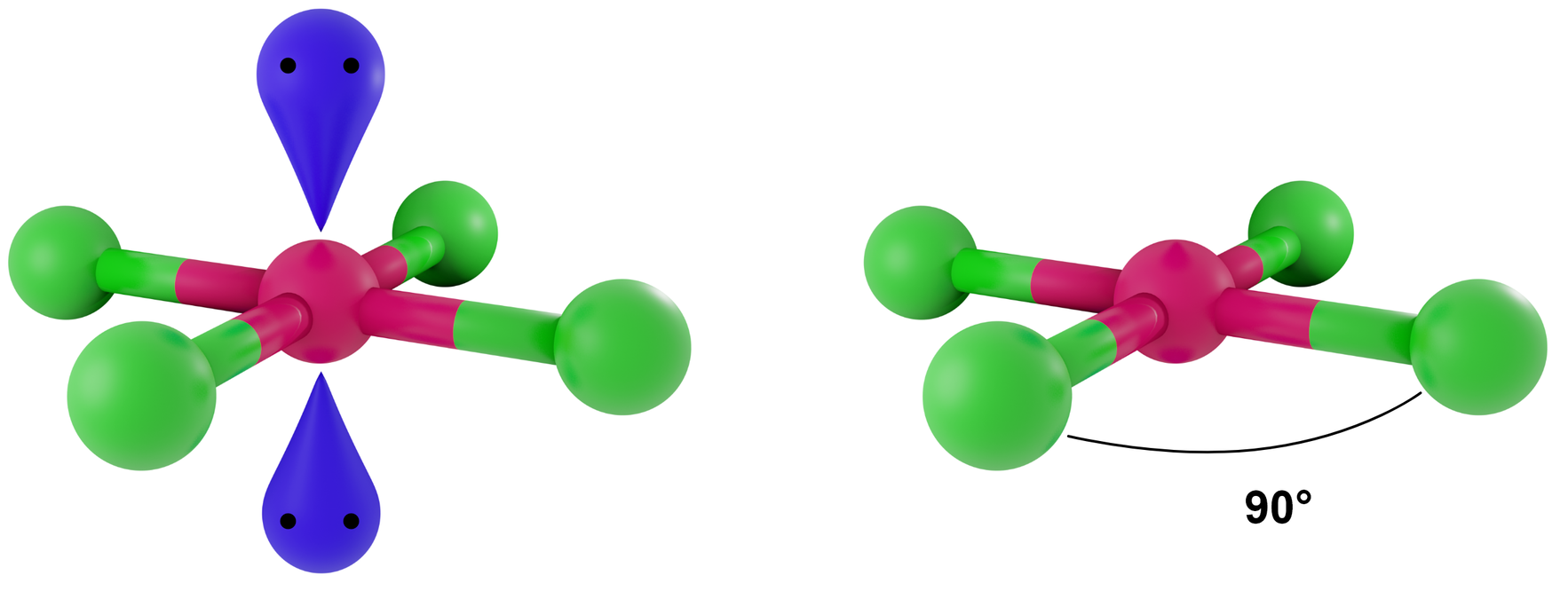
Przykłady: XeF4
Liczba przestrzenna 7, symetria kierunków orbitalnych bipiramidy pentagonalnej
- dla LwpE = 0 - bipiramida pentagonalna
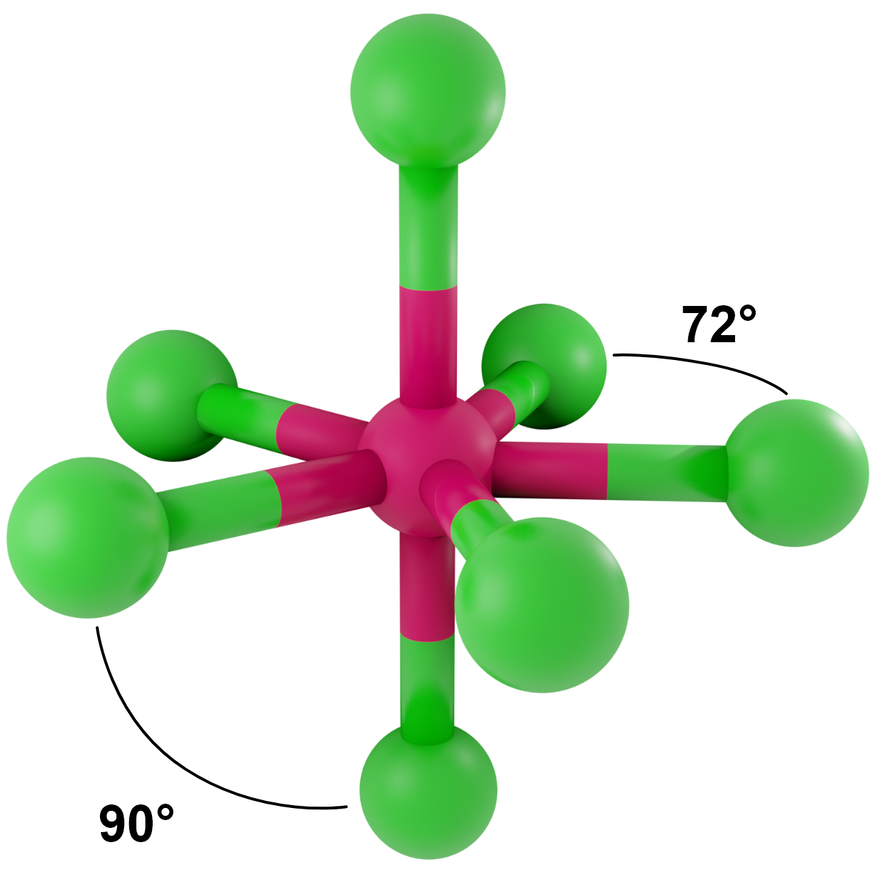
Przykłady: IF7
- dla LwpE = 1 - zdeformowana bipiramida pentagonalna, piramida pentagonalna
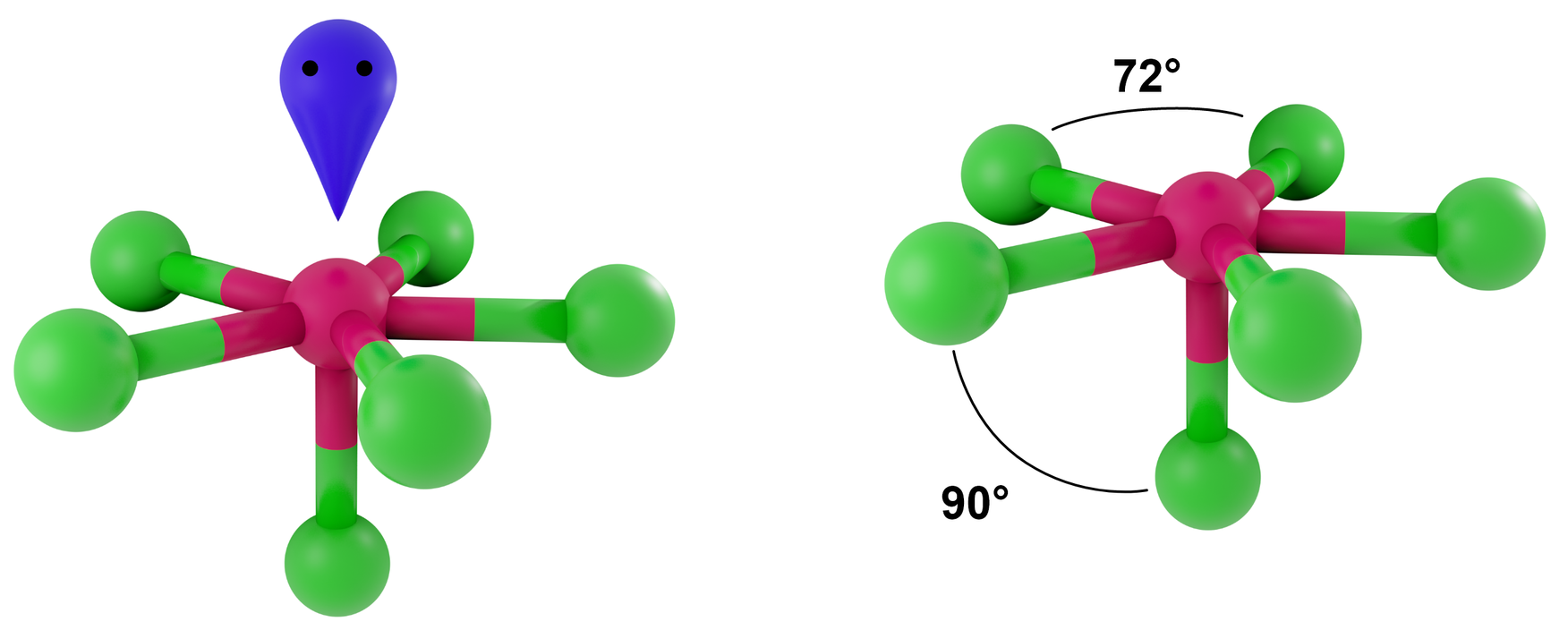
Przykłady: SeBr62-
_________________Grafiki: Kształt cząsteczek lub jonów dla poszczególnych liczb przestrzennych*. Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.
* Wykorzystano grafiki zamieszczone na Zintegrowanej Platformie Edukacyjnej.
