1.4.5 Graficzny zapis orbitalu
Obrazem graficznym orbitalu jest fragment przestrzeni, w której prawdopodobieństwo znalezienia elektronu jest duże. Każdy orbital ma inny kształt i orientację przestrzenną (rys. 9-11), a zajmujący go elektron charakteryzuje się inną energia. Orbitale typu s mają kształt kuli.
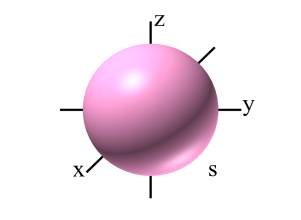
Rysunek 9. Orbital typu s.
Pozostałe orbitale wykazują orientację przestrzenną, co znaczy, że niektóre kierunki w przestrzeni charakteryzują się wyższym prawdopodobieństwem spotkania elektronu. Np.: kształt orbitali p przypomina sferyczne ósemki nabite na poszczególne osie współrzędnych (rys. 10).
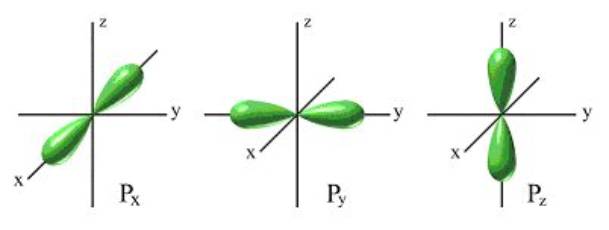
Rysunek 10. Orbitale typu p.
Istnieje znaczne prawdopodobieństwo spotkania elektronu wewnątrz tego orbitalu, niż na zewnątrz. Ale prawdopodobieństwo zajęcia orbitalu px, py lub pz jest takie samo. Każda „ósemka” ma tę samą charakterystykę energetyczną; żadna z nich nie jest uprzywilejowana, prawdopodobieństwo obsadzenia każdej nich przez elektron jest dokładnie takie samo. Takie orbitale nazywa się zdegenerowanymi. Orbital p jest trójkrotnie zdegenerowany, ze względu na równocenność energetyczną orbitali px, py i pz. Analogicznie orbital d (rys.11) jest pięciokrotnie zdegenerowany, a f siedmiokrotnie.
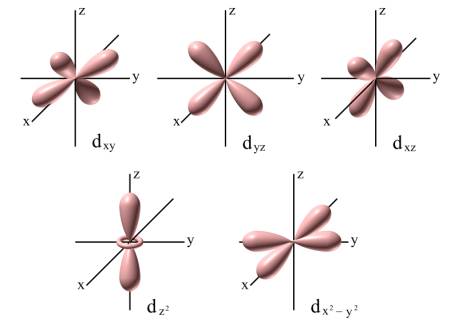
Rysunek 11. Orbitale typu d.
Każdy orbital może pomieścić dwa elektrony. Muszą się one różnić liczbą spinową. Liczba spinowa s jest czwartą liczbą kwantową. Może przyjąć tylko dwie wartości: -1/2 lub +1/2. Na jednym orbitalu nie mogą się znajdować dwa elektrony o jednakowej liczbie spinowej. Zasada ta jest znana jako zakaz Pauliego: W atomie nie mogą znajdować się dwa elektrony charakteryzowane jednakowym zestawem liczb kwantowych.
Przedstawiając zakaz Pauliego stosuje się niekiedy „klatkowy” zapis orbitali. Zajęte orbitale są przedstawiane w postaci kwadratów zawierających strzałki o zwrotach zgodnych lub przeciwnie skierowanych. Jest to umowny sposób przedstawiania elektronów o tych samych lub przeciwnych liczbach spinowych. Zakaz Pauliego zabrania obecności dwu elektronów o tych samych spinach na jednym i tym samym orbitalu:
![]()
Prawidłowy zapis powinien wyglądać następująco:
![]()
Powyższy zapis odnosi się do orbitalu trójkrotnie zdegenerowanego zajętego przez 5 elektronów.