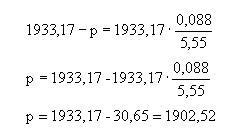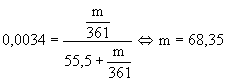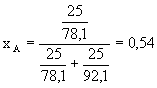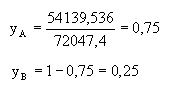4.4 Przykłady obliczeń
| 1.
Jaką prężność pary wykazuje roztwór 30 g sacharozy
|
|||||||
|
Rozwiązanie: Masa molowa sacharozy wynosi 342,3g/mol 30g sacharozy stanowi 30/342,3 = 0,088 mola 100g wody stanowi 100/18,02=5,55 mola Względne obniżenie prężności pary nasyconej nad roztworem (1933,17-p)/1933,17 równe jest stosunkowi liczby moli substancji rozpuszczonej do liczby moli rozpuszczalnika czyli 0,088/5,55 czyli:
Odpowiedź: Prężność pary nasyconej nad roztworem wynosi 1880,92 Pa.
|
|||||||
| 2. 1000g wody rozpuszczono 70g substancji o masie molowej 361g /mol. Oznaczona w 20oC prężność pary nasyconej nad roztworem wynosi 2326,47 Pa. Prężność pary wodnej w tej temperaturze wynosi 2334,47 Pa. Jaka była masa substancji rozpuszczonej ? | |||||||
|
Rozwiązanie: Względne obniżenie prężności pary nasyconej nad roztworem wynosi : odpowiada to ułamkowi molowemu rozpuszczonej substancji :
Odpowiedź:. Masa substancji rozpuszczonej wynosi 68,35g.
|
|||||||
|
3.
Sporządzono roztwór złożony z 25g benzenu
|
|||||||
|
Rozwiązanie: masa molowa benzenu wynosi 78,1g/mol masa molowa toluenu wynosi 92,1g/mol ułamek molowy benzenu w roztworze wynosi:
Prężność pary nasyconej nad roztworem równa się sumie cząstkowych prężności par obu składników. Każda z cząstkowych prężności par stanowi iloczyn prężności pary nasyconej składnika i jego ułamka molowego w roztworze:
Ułamek molowy składnika w fazie gazowej równy jest stosunkowi cząstkowej prężności pary składnika do całkowitej prężności pary nasyconej nad roztworem :
Odpowiedź:. Skład fazy gazowej jest następujący: benzen 75%, toluen 25%.
|
|||||||
| 4.
Jaka jest prężność pary nasyconej w temperaturze 40oC
nad roztworem zawierającym 18g acetonu
|
|||||||
|
Rozwiązanie: masa molowa acetonu wynosi 48g/mol masa molowa dwusiarczku węgla wynosi 76g/mol ułamek molowy acetonu w roztworze wynosi :
Odpowiedź:. Prężność pary nasyconej nad roztworem wynosi 66421,21 Pa.
|
|||||||