Wiązania chemiczne
5. Wiązania jonowe
Wiązanie jonowe powstają wówczas gdy, atomy dwóch łączących się pierwiastków zyskują konfigurację elektronową gazów szlachetnych dzięki temu, że atomy pierwiastka określanego jako elektrododatni tracą swoje elektrony walencyjne na rzecz atomów drugiego pierwiastka – elektroujemnego
Wytworzone w ten sposób jony, dodatni (kation) i ujemny (anion), przyciągają się dzięki działaniu sił elektrostatycznych
Jednym z najlepiej poznanych związków o budowie jonowej jest chlorek sodu. Poniżej przedstawiono mechanizm powstawania wiązania między atomem sodu, a atomem chloru:
- w ujęciu graficznym
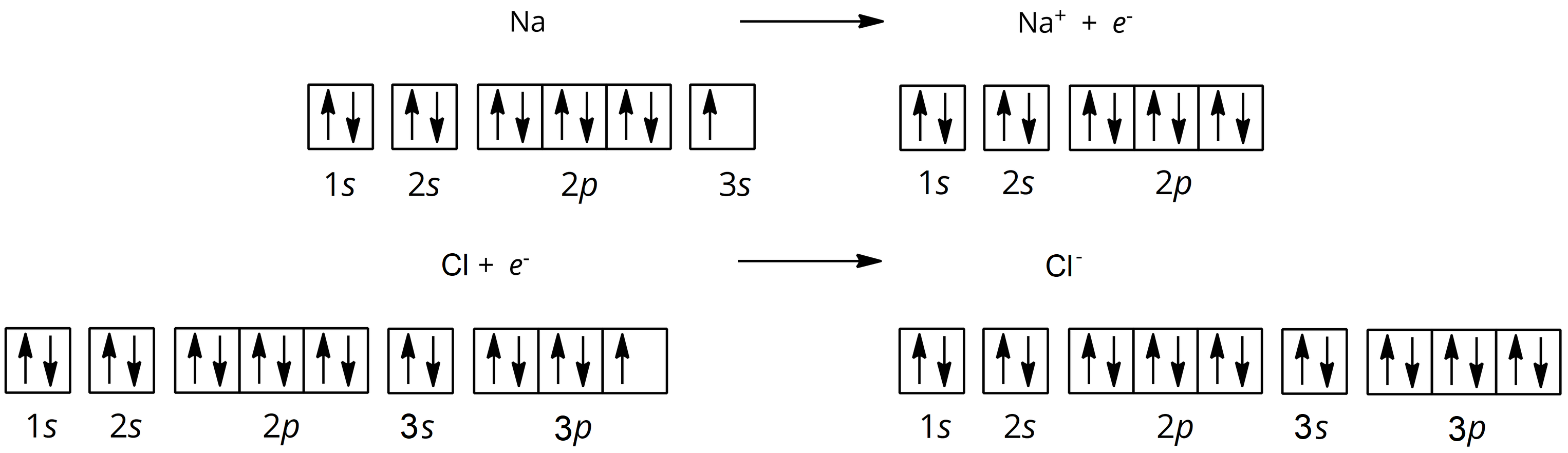
Grafika: oprac. Sylwia Zelek-Pogudz, licencja CC BY-SA 4.0. [na podst. Zapis graficzny tworzenia wiązania jonowego z wykorzystaniem orbitali*. Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0].
- w ujęciu powłokowym
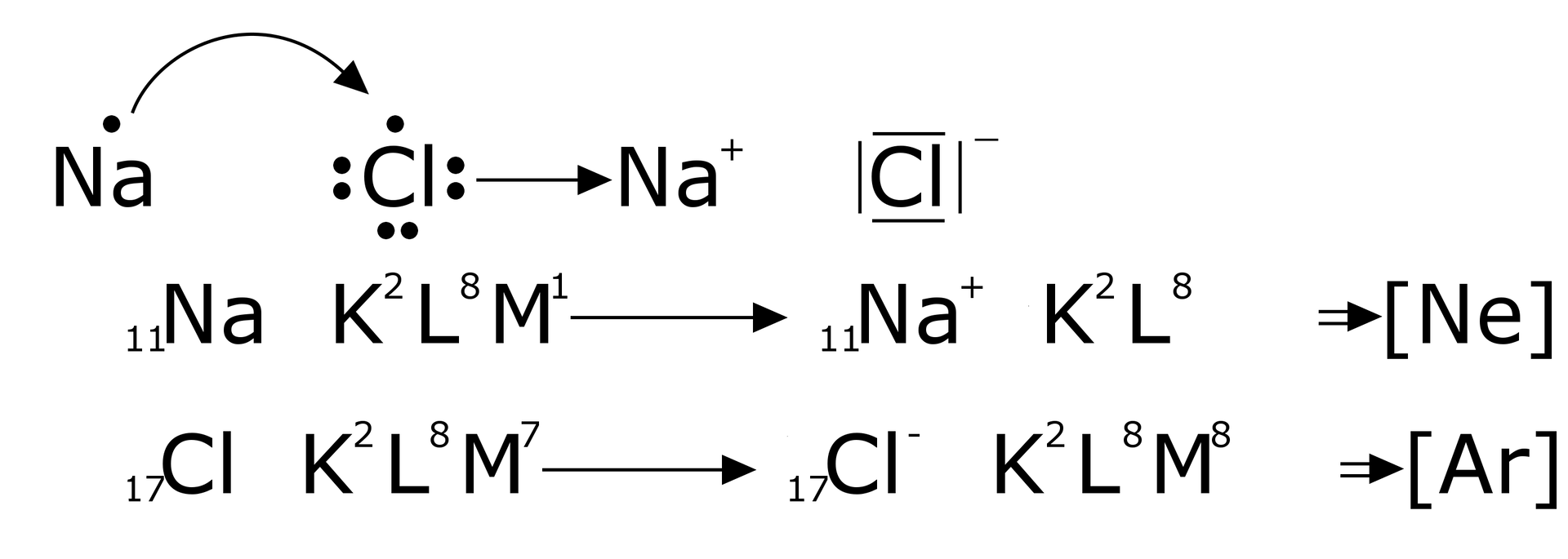
Grafika: Tworzenie jonów dodatnich oraz ujemnym w ujęciu powłokowym*. Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.
Ważne!
Należy pamiętać, że nie istnieją pojedyncze cząsteczki związku jonowego. Wzór sumaryczny takiego związku (np. CaO, NaCl) określa rodzaj jonów w sieci krystalicznej oraz ich stosunek ilościowy.
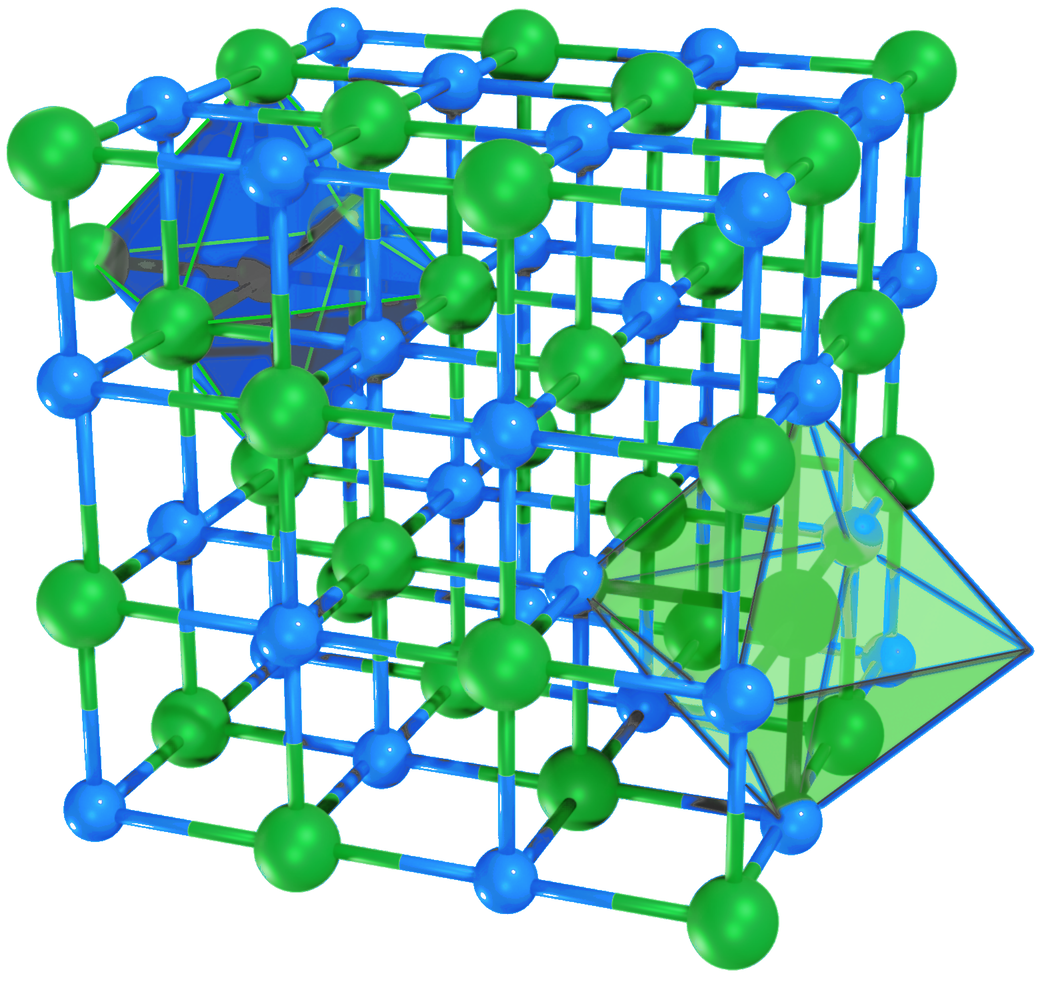
Grafika: Fragment sieci krystalicznej chlorku sodu*. Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.
 Nurtuje Cię pytanie: "Jak powstają wiązania jonowe?* Obejrzyj animacje, może uzyskasz odpowiedź na nie
Nurtuje Cię pytanie: "Jak powstają wiązania jonowe?* Obejrzyj animacje, może uzyskasz odpowiedź na nie
Animacja: Jak powstają wiązania jonowe?*. Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.
Wiązanie jonowe, niezależnie od wartości różnicy elektroujemnosci występuje m.in. w:
tlenkach metali aktywnych, np. Na2O, MgO,
wodorkach litowców i berylowców (z wyjątkiem berylu i magnezu), np. NaH, CaH2,
wodorotlenkach metali aktywnych, np. LiOH, KOH,
solach metali aktywnych, np. NaCl, NaNO3.
* Wykorzystano grafiki zamieszczone na Zintegrowanej Platformie Edukacyjnej.

